研究内容の紹介
有機分子の構造は無数にありますが、有機合成化学の技術を使えば、天然に存在しない有機分子を人工的に設計して合成することができます。
私たちの研究室では、世界初の「オリジナル分子」を合成する研究をしています。新しい構造をもつ分子は、新しい機能をもつことが多く、分子の合成と機能の解明を並行しながら研究を進めています。特に、「発光」と「キラル」に関連する機能をもった分子の研究に取り組んでいます。
1. こすると発光色が変わる!メカノクロミック発光分子の合成
有機発光分子は、外部から加えられた光や電界などのエネルギーを、光エネルギーとして効率良く放出することのできる分子です。発光現象は、身近なところではテーマパークの再入場スタンプや、紙幣の偽造防止印刷、有機ELディスプレイなどに使われています。
私たちは、別の目的で合成した新分子が、「こする」などの機械的刺激を加えることで固体状態での発光色が可逆的に変化する「メカノクロミック発光(MCL: Mechanochromic Luminescence)」を示すことを偶然見出しました。これをきっかけとして、「どのような分子がメカノクロミック発光を示すのか」を解明するとともに、メカノクロミック発光を望み通りに実現することを目指した研究を進めています1–3)。
- Ito, S.* Chem. Lett. 2021, 50, 649–660 (Invited Review, Open Access).
- Ito, S.* J. Photochem. Photobiol., C 2022, 51, 100481 (Invited Review, Special Issue on Soft Crystals).
- Ito, S.* CrystEngComm 2022, 24, 1112–1126 (Invited Review, Selected as Front Cover, Selected as HOT article).
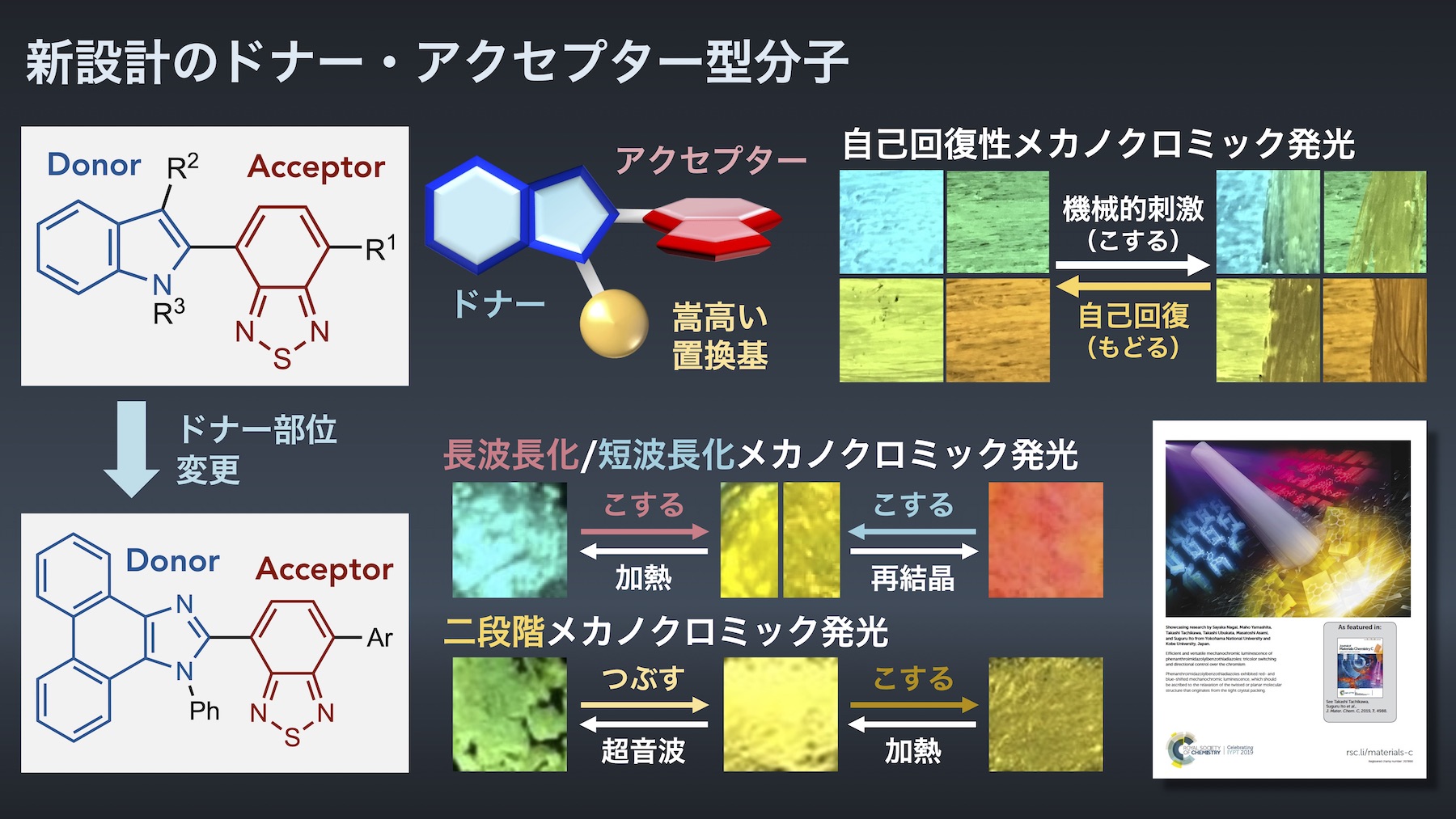
(1) ドナー・アクセプター型分子のメカノクロミック発光
従来のメカノクロミック発光分子は、機械的刺激を加えると発光波長が長波長化し、加熱や有機溶媒の曝露で元に戻る2色間変化を示します。私たちは、電子アクセプター性のベンゾチアジアゾール環に電子ドナー性の複素環を直接結合する新設計のドナー・アクセプター型分子を開発しています。
最初に発見したドナー部位がインドール環の誘導体は、発光色が室温で自己回復するメカノクロミック発光を示しました4,5)。さらに、ドナー部位をフェナントロイミダゾール環とすることで、こすると短波長化するメカノクロミック発光や、機械的刺激の強さの違いに応じて二段階で発光色が変化するメカノクロミック発光を実現しています6)。
- Ito, S.*; Yamada, T.; Taguchi, T.; Yamaguchi, Y.; Asami, M. Chem. Asian J. 2016, 11, 1963–1970 (Link).
- Ito, S.*; Taguchi, T.; Yamada, T.; Ubukata, T.; Yamaguchi, Y.; Asami, M. RSC Adv. 2017, 7, 16953–16962 (Open Access).
- Nagai, S.; Yamashita, M.; Tachikawa, T.*; Ubukata, T.; Asami, M.; Ito, S.* J. Mater. Chem. C 2019, 7, 4988–4998 (Link, Selected as Inside Back Cover, Most Popular Article 2019).
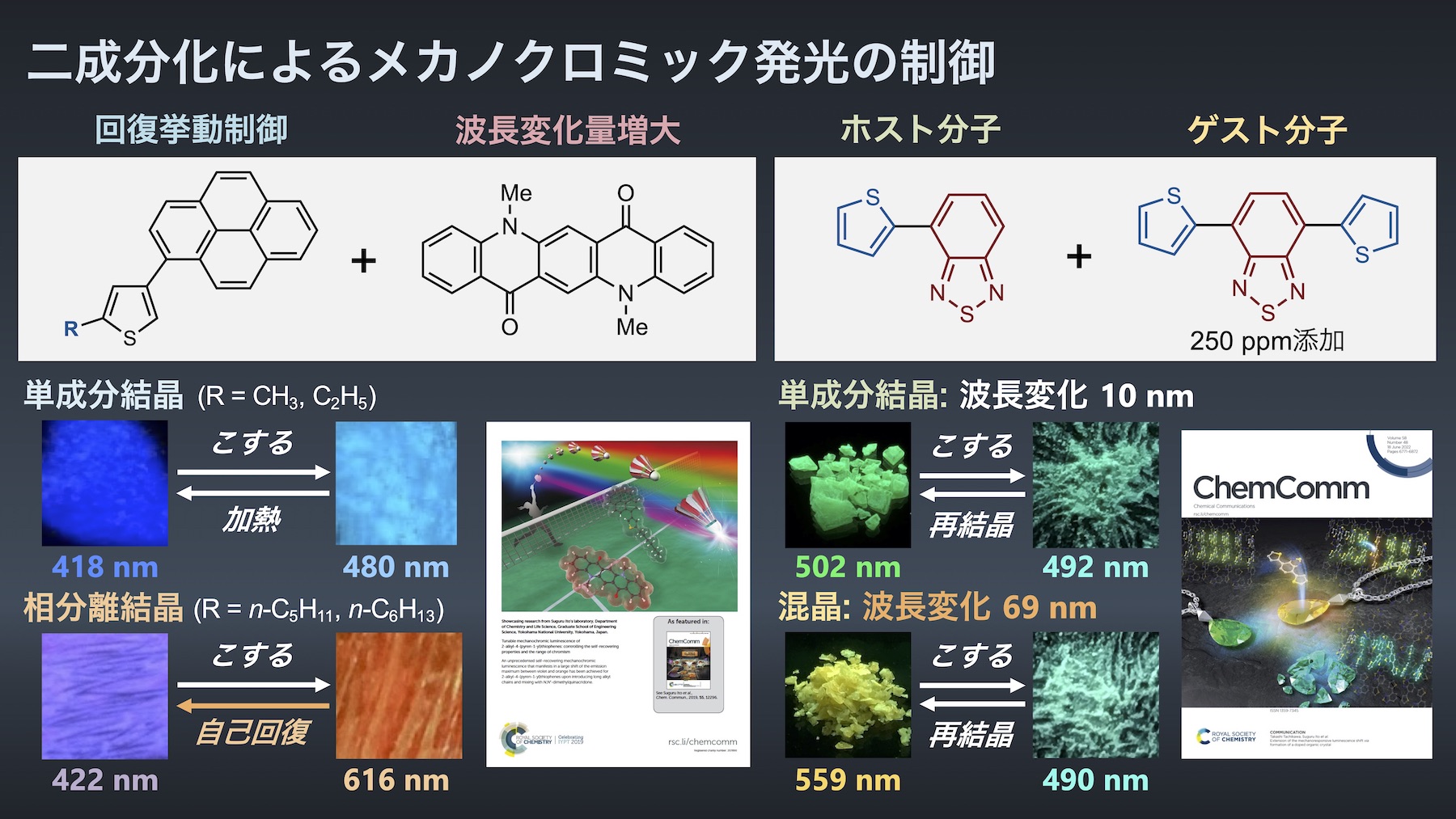
(2) メカノクロミック発光分子の二成分化
これまでに開発されたメカノクロミック発光分子は、大部分が単成分からなる結晶でした。私たちは、メカノクロミック発光分子を別の発光分子と二成分化することで、メカノクロミック発光挙動を合理的に制御する手法について研究しています。
ピレン環をもつ発光分子は、置換基Rを伸ばすと機械的刺激付与後に発光色が自己回復するようになり、ジメチルキナクリドンと混合して相分離状態の結晶とすることで、発光波長の変化量を約200 nmまで拡大することができました7)。別の組合せの相分離結晶では発光波長変化量340 nmを達成しています8)。また、緑色発光するホスト分子結晶に、ゲスト分子を極微量(250 ppm)添加して混晶とすることで、機械的刺激付与時の波長変化量を10 nmから69 nmに拡大することにも成功しています9)。
- Ikeya, M.; Katada, G.; Ito, S.* Chem. Commun. 2019, 55, 12296–12299 (Link, Selected as Back Cover, Press Release).
- Ito, S.*; Sekine, R.; Munakata, M.; Yamashita, M.; Tachikawa, T.* Chem. Eur. J. 2021, 27, 13982–13990 (Read Only Link, Selected as Cover Feature).
- Yoshida, R.; Tachikawa, T.*; Ito, S.* Chem. Commun. 2022, 58, 6781–6784 (Link, Selected as Front Cover).
2. 右手と左手の化学 〜キラル分子の新機能に向けて〜
右手と左手のように互いに重ね合わせることのできないキラル分子は、右手型が薬になっても左手型は毒になるなど、異なる生物活性を示すことから、生命科学分野において長年研究されています。通常の有機合成では、キラルな分子の右手型と左手型は1:1の割合で得られますが、「不斉合成」の技術を用いれば、右手分子と左手分子を作り分けることができます。
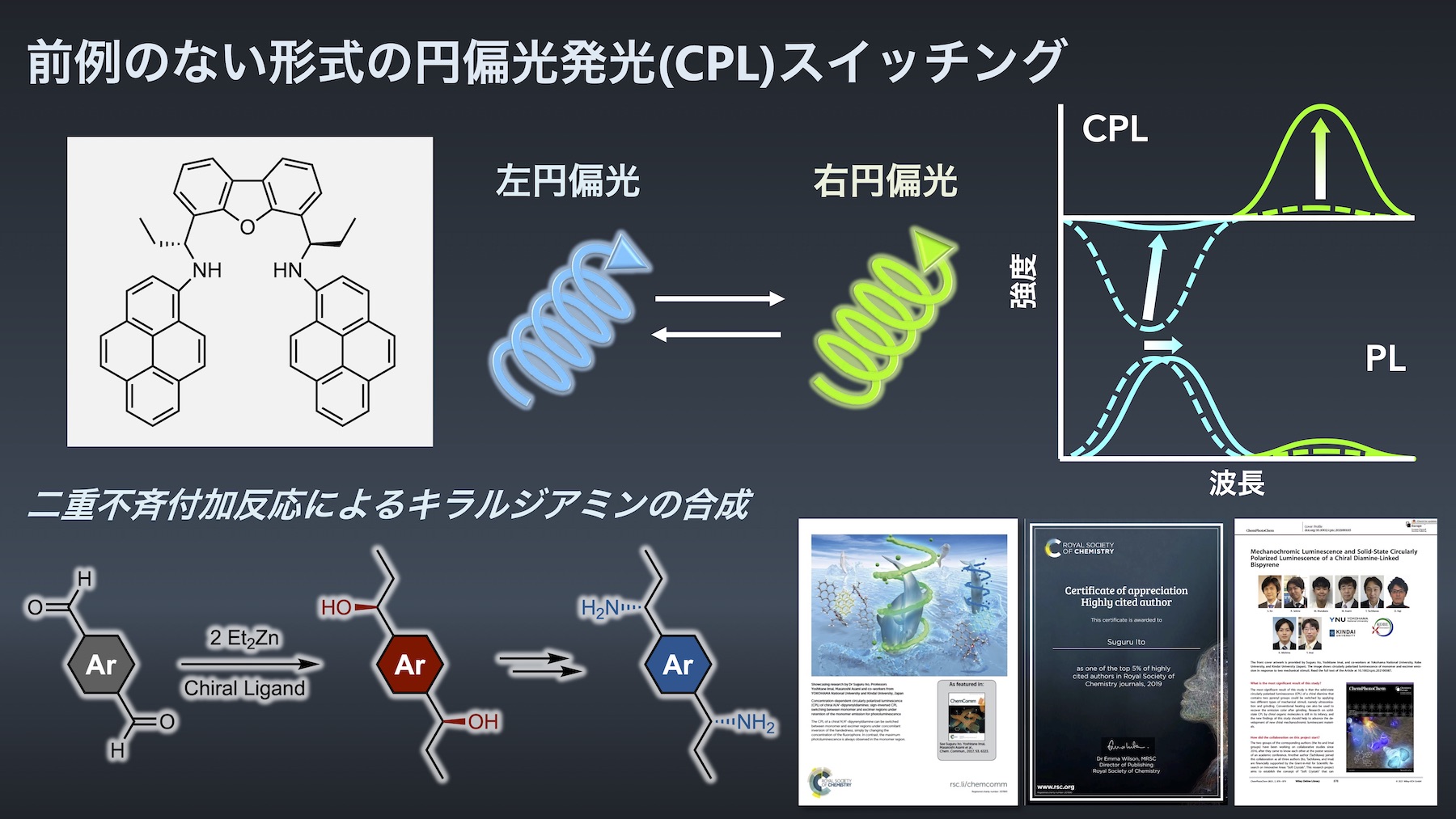
私たちは、2箇所の不斉中心を一挙に構築する「二重不斉付加反応」によりキラルなジオール分子を高立体選択的に得る手法を確立しました10)。得られたキラルジオールは容易にキラルジアミンに変換することができます。この手法を利用して、新機能をもつキラル分子を開発することを目的とした研究に取り組んでいます。
代表的な成果としては、発光性のキラル分子を不斉合成することで、前例の無い形式で円偏光発光(CPL: Circularly Polarized Luminescence)をスイッチングすることに成功しています11)。CPLは、3次元ディスプレイや暗号通信などへの応用が近年注目されています。私たちの開発した分子では、従来のCPL分子とは異なり、見た目の発光(PL: Photoluminescence)はそのままに、CPLの回転方向と波長を同時に切り替えることができます。また、2種類の機械的刺激に応答して固体CPLが可逆的に変化するキラル分子を開発することにも成功しています12)。現在は、より高度なCPL機能をもったキラル分子の合成に挑戦しています。
- Ito, S.*; Ikeda, K.; Asami, M.* Chem. Lett. 2016, 45, 1379–1381 (Link).
- Ito, S.*; Ikeda, K.; Nakanishi, S.; Imai, Y.*; Asami, M.* Chem. Commun. 2017, 53, 6323–6326 (Link, Selected as Back Cover, Top 5% highly cited, Press Release, ChemStation, 財経新聞).
- Ito, S.*, Sekine, R.; Munakata, M.; Asami, M.; Tachikawa, T.; Kaji, D.; Mishima, K.; Imai, Y.* ChemPhotoChem 2021, 5, 920–925 (Read Only Link, Selected as Front Cover, Highlighted in Cover Profile).